Công thức tính hiệu suất phản ứng hóa học
Dạy học tốt xin gửi tới các bạn nội dung Công thức tính hiệu suất phản ứng hóa học và file đính kèm để các bạn tiện tải về sử dụng. Chúc các bạn có được những thông tin như mong muốn của mình. Nào hãy cùng xem nội dung ngay bên dưới nhé.
- Các văn bản, tài liệu có thể bạn quan tâm:
- 10 Mẫu lời cảm ơn tiểu luận, luận văn ấn tượng nhất
- 100 câu đố vui có đáp án
- 101+ câu đố trong nhanh như chớp (có đáp án)
Công thức tính hiệu suất phản ứng hóa học
I. Công thức tính hiệu suất của phản ứng hóa học
1. Công thức tính hiệu suất của phản ứng hóa học và ví dụ cụ thể
Cho phản ứng hóa học: A+B–>C
Hiệu suất phản ứng:
H = số mol pứ . 100% / số mol ban đầu
hoặc cũng có thể tính theo khối lượng:
H = khối lượng thu được thực tế . 100% / khối lượng thu được tính theo phương trình
Lưu ý là tính hiệu suất theo số mol chất thiếu (theo số mol nhỏ)
Từ công thức cũng có thể tính được:
nC = nA pứ = (nAbđ . H)/100
nA bđ cần dùng: n Abđ = (nC.100)/H
2. Công thức tính khối lượng chất tham gia khi có hiệu suất
Do hiệu suất phản ứng nhỏ hơn 100%, nên lượng chất tham gia thực tế đem vào phản ứng phải hơn nhiều để bù vào sự hao hụt. Sau khi tính khối lượng chất tham gia theo phương trình phản ứng, ta có khối lượng chất tham gia khi có hiệu suất như sau:
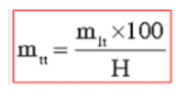
3. Công thức tính khối lượng sản phẩm khi có hiệu suất
Do hiệu suất phản ứng nhỏ hơn 100%, nên lượng sản phẩm thực tế thu được phải nhỏ hơn nhiều sự hao hụt. Sau khi khối lượng sản phẩm theo phương trình phản ứng, ta tính khối lượng sản phẩm khi có hiệu suất như sau:
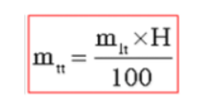
2. Ví dụ cụ thể:
Nung 0,1 mol CaCO3 thu được 0,08 mol CaO. Tính hiệu suất phản ứng hóa học xảy ra.
Trong bài này chúng ta có 2 cách để giải bài toán:
Cách 1:
CaCO3 ——–> CaO + CO2
0,1 mol —-> 0,1 mol
Theo phản ứng ta có 0,1 mol CaCO3 tạo 0,1 mol CaO. Tuy nhiên theo thực tế đo được chỉ thu được 0,08 mol CaO. Như vậy đối với CaO lượng tính toán theo phản ứng là 0,1 (gọi là khối lượng theo lý thuyết) và lượng chắc chắn thu được là 0,08 (gọi là lượng thực tế). Hiệu suất phản ứng H(%) = (thực tế/lý thuyết)*100 = (0,08/0,1)*100 = 80%, tức là:
Cách 2:
CaCO3 ——–> CaO + CO2
0,08 mol <——0,08mol
Nhìn tỉ lệ mol trên phương trình nếu thu được 0,08 mol vôi sống CaO cần dùng 0,08 mol CaCO3. Tuy nhiên đề bài cho là nung 0,1 mol CaCO3. Tóm lại đối với CaCO3 lượng tính toán theo phản ứng là 0,08 (gọi là lựong lý thuyết) và lượng chắc chắn cần phải có là 0,1 (gọi là lựong thực tế). Hiệu suất phản ứng H= lý thuyết/thực tế)*100 = (0,08/0,1)*100 = 80%
Vậy tóm lại khi tính hiệu xuất phản ứng thì chúng ta cần xác định xem mình dựa vào tác chất hay sản phẩm để có công thức phù hợp để tính.
+ Nếu dựa vào sản phẩm thì công thức: H = (thực tế/lý thuyết)*100
+ Nếu dựa vào tác chất thì công thức: H = (lý thuyết/thực tế)*100
Theo kinh nghiệm của tôi với các bài tập tính toán hiệu suất phản ứng, khi làm bài đừng để ý đến thực tế, lý thuyết gì cả. Cứ thực hiện tính toán bình thường, dựa vào tác chất hay sản phẩm tùy ý, sau đó đối chiếu lượng ở đề bài cho xem giá trị nào lớn, giá trị nào nhỏ.
Hiệu suất = (giá trị nhỏ/giá trị lớn)*100
II. Bài tập tính hiệu suất phản ứng
Bài tập 1: Tính khối lượng Na và thể tích khí Cl2 cần dùng để điều chế 4,68 gam muối Clorua, nếu hiệu suất phản ứng là 80%
Lời Giải:
n NaCl = m NaCl/ M NaCl = 4,68/58,5 = 0,08 (mol)
Phương trình hóa học:
2Na + Cl2 → 2NaCl
từ pt => số mol Na = 0,08*100/80 = 0,1 (mol)
n Cl2 = (0,08*100)/2*80 = 0,05 (mol)
m Na = 0,1*23 = 2,3 (gam)
V Clo = 0,05*22,4 = 1,12 (lit)
Bài tập 2: Cho 19,5 gam Zn phản ứng với 7 (l) clo thì thu được 36,72 gam ZnCl2. Tính hiệu suất của phản ứng?
Bài Giải
n Zn = 19,5/65 = 0,3 (mol)
n Cl2 = 7/22,4 = 0,3125 (mol)
n ZnCl2 = 0,27 (mol)
Zn + Cl2 → ZnCl2
Ta thấy:
n Cl2 > n Zn => so với Cl2 thì Zn là chất thiếu, nên ta sẽ tính theo Zn.
Từ phương trình => n Zn phản ứng = n ZnCl2 = 0,27 (mol)
Hiệu suất phản ứng: H = số mol Zn phản ứng *100/số mol Zn ban đầu = 0,27 * 100/0,3 = 90 %
Xem và tải các văn bản tài liệu khác
- 120 câu bài tập word form thi vào 10
- 14 điều tuyệt vời mà đậu tương mang lại cho sức khỏe của bạn
- 150 câu hỏi thi bằng lái xe máy A1 mới nhất
- 16 hình nền 4D đẹp và độc đáo
- 20-10 tặng quà gì cho mẹ ý nghĩa và đặc biệt nhất
- 27 biểu hiện suy thoái
- 3 cách viết số mũ trong Word 2010,2013,2016
- 37 trò chơi tập thể BỰA mà VUI trong phòng tiệc tất niên cuối năm công ty
- 5 điều Bác Hồ dạy nhi đồng
- 7 ngôi chùa cầu duyên ở Việt Nam nổi tiếng
- 9 biểu hiện suy thoái về đạo đức lối sống
- BFF là gì? Trên Facebook mọi người viết BFF có nghĩa là gì? BF GF là gì?
- BFF là gì? Trên Facebook mọi người viết BFF có nghĩa là gì? BF GF là gì?
- Background Powerpoint Đẹp cho bài thuyết trình chuyên nghiệp
- Biên bản bàn giao nhà cho thuê chuẩn nhất
- Biên bản bàn giao tài liệu mới nhất
- Biên bản cam kết chịu trách nhiệm thông dụng.
- Biên bản cam kết không vi phạm mẫu chuẩn
- Biên bản chuyên đề sinh hoạt chi bộ cập nhật mới nhất
- Biên bản ghi chép sự việc hiện trường phổ biến nhất
- Xem tất cả các mẫu văn bản và tài liệu mẫu
