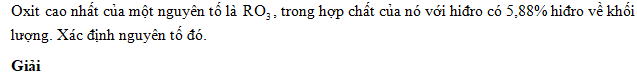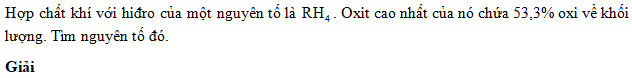Giải bài 10 trang 58 SGK Hóa học 10 Nâng cao
Hãy so sánh tính kim loại của Mg (Z = 12) với Na(Z = 11) và Al(Z = 13).
Hãy so sánh tính kim loại của Mg (Z = 12) với Na(Z = 11) và Al(Z = 13).
Giải
Cấu hình electron nguyên tử của các nguyên tố:
\(\eqalign{
& Na\left( {Z = 11} \right)\,\,1{s^2}2{s^2}2{p^6}3{s^1} \cr
& Mg\left( {Z = 12} \right)\,\,1{s^2}2{s^2}2{p^6}3{s^2} \cr
& Al\left( {Z = 13} \right)\,\,1{s^2}2{s^2}2{p^6}3{s^2}3{p^1} \cr} \)
Nguyên tử của 3 nguyên tố trên đều có 3 lớp electronn nên chúng đều thuộc chu kì 3. Chúng lần lượt có số electron lớp ngoài cùng la 1, 2, 3 nên đều là những kim loại. Theo quy luật về sự biến đổi tính kim loại-phi kim, Mg có tính kim loại yếu hơn Na nhưng mạnh hơn Al.
Trên đây là bài học "Giải bài 10 trang 58 SGK Hóa học 10 Nâng cao" mà dayhoctot.com muốn gửi tới các em. Để rèn luyện về kỹ năng làm bài thi và kiểm tra các em tham khảo tại chuyên mục "Đề thi học kì 1 lớp 10" nhé.
Nếu thấy hay, hãy chia sẻ tới bạn bè để cùng học và tham khảo nhé! Và đừng quên xem đầy đủ các bài Giải bài tập Hóa Học Lớp 10 của dayhoctot.com.
Các bài học liên quan
Tổng số hạt proton, nơtron, electron của các nguyên tử một nguyên tố thuộc nhóm VIIA là 28.
a) Tính nguyên tử khối.
b) Viết cấu hình electron nguyên tử của nguyên tố đó.
Oxit cao nhất của một nguyên tố là , trong hợp chất của nó với hiđro có 5,88% hiđro về khối lượng. Xác định nguyên tố đó.
Hợp chất khí với hiđro của một nguyên tố là . Oxit cao nhất của nó chứa 53,3% oxi về khối lượng. Tìm nguyên tố đó.
Khi cho 0,6g một kim loại nhóm IIA tác dụng hết với nước tạo ra 0,336 lít khí hiđro (ở điều kiện tiêu chuẩn). Xác định kim loại đó.
Hai nguyên tố A và B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn có tổng số đơn vị điện tích hạt nhân la 25.
a) Viết cấu hình electron để xác định hai nguyên tố A và B thuộc chu kì nào, nhóm nào.
b) So sánh tính chất hóa học của chúng.
Cho 8,8g một hỗn hợp hai kim loại nằm ở hai chu kì liên tiếp nhau và thuộc nhóm IIIA, tác dụng với HCl dư thì thu được 6,72 lít khí hiđro ở điều kiện tiêu chuẩn. Dựa vào bảng tuần hoàn hãy cho biết tên của hai kim loại đó.
Nguyên tố X có cấu hình electron như sau: . Hãy xác định:
a) Vị trí của X trong bảng tuần hoàn.
b) Nêu tính chất hóa học cơ bản của X.
Các chương học và chủ đề lớn
Học tốt các môn khác lớp 10