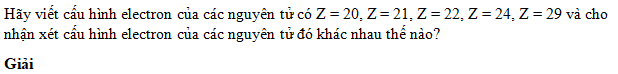Giải bài 4 trang 22 SGK Hóa học 10 Nâng cao
Biết rằng nguyên tố agon có ba đồng vị khác nhau, ứng với số khối 36, 38 và A. Phần trăm số nguyên tử của các động vị tương ứng lần lượt bằng: 0,34%; 0,06% và 99,6%. Tính số khối của đồng vị A của nguyên tố agon, biết nguyên tử khối trung bình của agon bằng 39,98.
Biết rằng nguyên tố agon có ba đồng vị khác nhau, ứng với số khối 36, 38 và A. Phần trăm số nguyên tử của các động vị tương ứng lần lượt bằng: 0,34%; 0,06% và 99,6%. Tính số khối của đồng vị A của nguyên tố agon, biết nguyên tử khối trung bình của agon bằng 39,98.
Giải
Nguyên tử khối trung bình của agon là:
\({\overline A _{Ar}} = {{36.0,34 + 38.0,06 + A.99,6} \over {100}} = 39,98 \Rightarrow A = 40.\)
Vậy các đồng vị của agon là: \(^{36}Ar\left( {0,34\% } \right);{\,^{38}}Ar\left( {0,06\% } \right);{\,^{40}}Ar\left( {99,6\% } \right).\)
Trên đây là bài học "Giải bài 4 trang 22 SGK Hóa học 10 Nâng cao" mà dayhoctot.com muốn gửi tới các em. Để rèn luyện về kỹ năng làm bài thi và kiểm tra các em tham khảo tại chuyên mục "Đề thi học kì 1 lớp 10" nhé.
Nếu thấy hay, hãy chia sẻ tới bạn bè để cùng học và tham khảo nhé! Và đừng quên xem đầy đủ các bài Giải bài tập Hóa Học Lớp 10 của dayhoctot.com.
Các bài học liên quan
Hãy cho biết tên của các lớp electron tương ứng với các giá trị của n = 1, 2, 3, 4 và cho biết các lớp đó lần lượt có bao nhiêu phân lớp electron.
Hãy cho biết số phân lớp electron, số obitan có trong lớp M và N.
Vẽ hình dạng obitan 1s, 2s và các obitan
Hãy ghép cấu hình electron ở trạng thái thái cơ bản của nguyên tử thích hợp
Sự phân bố electron trong nguyên tử tuân theo những nguyên lí và quy tắc gì? Hãy phát biểu các nguyên lí và quy tắc đó. Lấy thí dụ minh họa.
Tại sao trong sơ đồ phân bố electron của nguyên tử cacbon (C: ), phân lớp 2p lại biểu diễn như sau:
Hãy viết cấu hình electron của các nguyên tử có Z = 20, Z = 21, Z = 22, Z = 24, Z = 29 và cho nhận xét cấu hình electron của các nguyên tử đó khác nhau thế nào?
Các chương học và chủ đề lớn
Học tốt các môn khác lớp 10